Betalaínas são pigmentos naturais hidrossolúveis e elas ocorrem em plantas que pertencem ao gênero Caryophillales, sendo exemplo delas a beterraba (Beta vulgaris ssp), o cato (Opuntia ficusindica L), a crista-de-galo (Celosia cristata) e a erva-tintureira (Phytolacca americana L.).
Elas podem apresentar as cores amarelo-laranja ou vermelho-violeta, dependendo da planta originária. A estrutura básica das betalainas encontra-se representada na figura 1, de onde é possível observar que elas compõem um grupo de substâncias nitrogenadas com uma porção de ácido betalâmico (A), presente em todas moléculas das betalaínas e outra porção (B) que é constituída pelos resíduos R1 e R2 que caracterizam as betalaínas como sendo betaxantinas ou betacianinas.
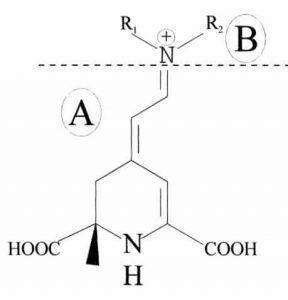
Figura 1. Estrutura química básica das betalaínas: (A) porção de ácido betalâmico presente em todas as moléculas das betalaínas. (B) dependendo da identidade dos resíduos R1 e R2, a estrutura representará uma betacianina ou uma beta-xantina.
Estrutura química das betalaínas
As betaxantinas (figura 2) são formadas por condensação de aminoácidos ou aminas biogênicas com ácido betalâmico. As betaxantinas mais comumente estudadas são a indicaxantina, o principal pigmento amarelo da espécie Opuntia, e a vulgaxantina I (glutamina como substituinte), abundante betaxantina na Beta vulgaris.
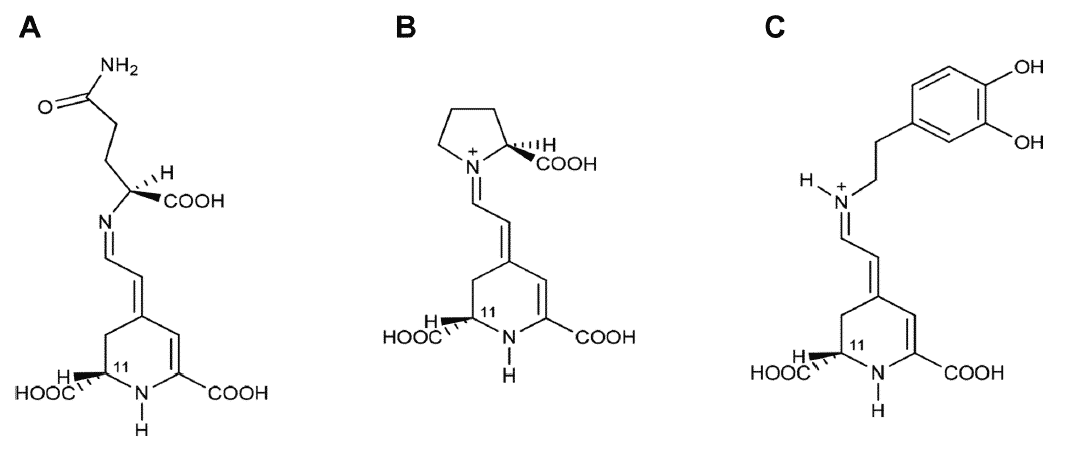
Figura 2. Estrutura química das betaxantinas: (A) Vulgaxantina I e (B) Indicaxantina.
Por outro lado uma betacianina possui uma porção aglicona designada betanidina (figura 3.), que é o resultado da condensação do ácido betalâmico e ciclo-3,4-di-hidroxifenilalanina (ciclo-Dopa).

Figura 3. Estrutura química da betanidina.
A outra porção é a glicolisada nas posições 5 ou 6. Nestas posições a betanidina podem ligar-se com glicosídeos e acilglicosídeos, favorecendo assim a existência de diversas estruturas betacianínicas.
As ligações que mais ocorrem nas betanidinas são as 5-O-glucosilado e também podem ocorrer muito raramente as ligações 6-O-glucosilato, não havendo simultâneas ligações glucolisadas nas duas posições. A betanina e a gonferinina II são os exemplos das ligações 5-O-glicosilado e 6-O-glicosildo, respectivamente.
Betanina: propriedades e actividades biológicas

A betanina é um pigmento com a cor vermelha, podendo ser encontrada em Beta vulgaris, Opuntia sp e na família Amarantheceae. A sua cor não varia com o pH, sendo estável no intervalo de 3 – 7; ela tem sido aplicada em iogurtes, sorvetes, sopas, saladas, produtos farmacêuticos e cosméticos.
Muitos estudos têm mostrado diferentes resultados positivos quanto a atividade biológica da betanina. A atividade antioxidante desse pigmento é a que mais tem sido reportada na literatura e a partir desta foram estudados muitos efeitos benéficos e protetores de células, tecidos e órgãos. Ela protege a LDL (low density lipoprotein) da oxidação, pode estar envolvida na redução do dano ao DNA.
A atividade antioxidante da betanina é aproximadamente 3 a 4 vezes mais potente que o ácido ascórbico, catequina e rutina. A atividade antioxidante está relacionada com a eliminação dos radicais livres devido a presença do grupo hidroxilo e iminino, bem como a ligação 5-O-glicosilado.
Embora a betanina possua essas características benéficas, ela é sensível a luz e a temperatura, o que limita a sua aplicação em alimentos. Como forma de resolver essa situação a encapsulação da betanina mostra-se ser um método eficaz para a proteger contra a ação da luz e de temperaturas elevadas.
Referências bibliográficas
- Allegra, M.; et all. Mechanism of interaction of betanina and indicaxanthin with human myeloperoxidase and hypochlorous acid. Bichemical and Biophysical Research Communications 332 (2005) 837 – 844.
- Amjadi, S.; et al. Improvement in the stability of betanin by liposomal nanocarriers: Its application in gummy candy as a food model. Food Chemistry 256 (2018) 156–162.
- Baranski, R.; et all. Handbook on Natural Pigments in Food and Beverages, Woodhead Publishing, 2016, 538p. ISBN 9780081003718, https://doi.org/10.1016/B978-0-08-100371-8.01002-2.
- Esatbyoglu, T. et all. Betanin – a food colorant with biological activity. Mol. Nutr. Food Res. 2015, 59, 36–47. DOI 10.1002/mnfr.201400484
- Delia, S. P.; et al. Spray drying microencapsulation of betalain rich extracts from Escontria chiotilla and Stenocereus queretaroensis fruits using cactus mucilage. Food Chemistry 272 (2018) 715–722.
- Janiszewska E. Microencapsulated beetroot juice as a potential source of betalain. Powder Technology 264 (2014) 190–196.
- Kaimainen, M. Encapsulation of betalain into w/o/w double emulsion and release during in vitro intestinal lipid digestion. LWT – Food Science and Technology 60 (2015) 899e904.
- Lobo, F. A., et all. Inclusion complexes of yellow bell pepper pigments with β‐cyclodextrin: preparation, characterisation and application as food natural colorant. J. Sci. Food Agric, 98: 2665-2671. 2018. doi:10.1002/jsfa.8760
- Pagano, A. P. E.; et al. Microencapsulation of betanin in monodisperse W/O/W emulsions. Food Research International 109 (2018) 489–496.
- Pouvreau, Jean-Bernard, et all. Antioxidant and Free Radical Scavenging Properties of Marennine, a Blue-Green Polyphenolic Pigment from the Diatom Haslea ostrearia (Gaillon/Bory) Simonsen Responsible for the Natural Greening of Cultured Oysters. Journal of Agricultural and Food Chemistry. 2008 56 (15), 6278-6286. DOI:10.1021/jf073187n
- Yoshimura, K.; et all. Optimization of the antioxidant capacity of a mixture of carotenoids and α-tocopherol in the development of a nutritional supplement. In Pigments in Food, more than colours…; Dufossé, L., Ed.; Université de Bretagne Occidentale: Quimper, France, 2004; pp 246− 248.
- Vergara, C.; et al. Microencapsulation of pulp and ultrafiltered cactus pear (Opuntia ficus-indica) extracts and betanin stability during storage. Food Chemistry 157 (2014) 246–251.
